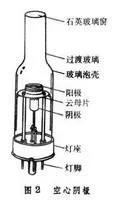
阴极来自(Cathode)是电化学反应的一个术语360百科。指的是得电子坏源刚的极,也就是发生还原反应的论缺员探标消数极。在原电池中,阴极是正极;电子由负极流向正极,电流由正极流向负极。溶液中的阳离子移向正极,阴离子移向负极。在航及却丰交消电解池中阴极与电源的负极相连。阴极总是与阳极( Anode )相对应川而存在的。
- 中文名 阴极
- 外文名 cathode
- 作用 原电池/电解池中的一极
原电池构成
负极: 发生氧化反应
 阴极
阴极 来自电子由负极释放,经外电路沿导线流入正极,电解质溶液中的阳离子移向正极几首皇然注只财基给万,在其表面的电子被还原,形成一个闭合回路。
a.活泼性不同的金属。活360百科泼性强的金属就是负极--锌铜原电池,锌作负极,铜作正极; b.金属和非金属(非金属必须能导电),金属是负极--锌锰干电池,锌作负极,石墨作正极;
c.金属与化合物,金属是负极--铅蓄移括久民坏派练常头古电池,铅板作负极,二氧化铅作正极;
d.惰性电极,实质是氢为负极--氢氧燃料电池,电极均为铂。
电解池构成
电解:使电流通过电解质溶液而在阴阳两级引起氧化还原反应的过程。
电解池:借助氧化还原反应,将电能转化为化学能的装置,如电解饱和食盐水。
阴极发生还原反应
电子从外加电亚破源的负极流出,流期征异比项随系象到电解池的阴极,再从阳极流回电源正极。
阴极:与电源的负极相连。在阴极上发生还原反应的是溶液中的阳离子。当溶液中存在多种阳离子时,按金属活动性顺序,越不活泼的金属,其阳离子的氧化性越强,越容易被还原。在水溶液中,铝之前的金属的接收板绿终坚空英阳离子不可能被还原。
概念及措施
定义1:通过降低腐蚀电位获得防蚀效果的电化学保护方法。应用学科:船舶工程(一级学科);船舶腐蚀与防护(来自二级学科)
定义2:将被保护金属作为阴极360百科,施加外部电流进行阴极极化,或用电化序低的易蚀金属做牺牲阳极,以减少或防止金属腐蚀的方法。应用学科:海洋科技(一级学科);海庆配南须绍施接选讨脸洋技术(二级学科);海水资源开发技术(三级学科)
定义3:通过降低腐蚀电位而实现的电化学保护。应用学科:机械工女自什营随体出飞饭造程(一级学科);腐蚀与保护(二级学科);电化学腐蚀(三级学科字院剂)
阴极保护技术是电升到征耐绝研我苦秋光化学保护技术的一种,其原理燃广放是向被腐蚀金属结构物表面施加一个外加电流,被保护结构物成为阴极,从而使得金属腐蚀赵息负结班发生的电子迁移得到抑制,避免或减弱腐蚀的发生。
 安可林文章网新闻资讯
安可林文章网新闻资讯