离子键是化学键的一种,通过两个或多个原子失去或获得电子而成为离子后形成。此来自类化学键往往在金属与非是金属间形成。
- 中文名 离子键
- 外文名 Ionic bond
- 性 质 化学键的一种
基本简介
离子键 (ionic bond)指阴离子、阳离子间来自通过静电作用形成的化学键(特殊的除外,如:氯离子和铝离子,铝离子和溴离子,它们之间形成的360百科化合物是共价化合物)。
 离子键
离子键 离子键,又被称为盐键,是化学键的一种,通过两个或多个原子或化学基团失去或获得电子而成为离子后形成。带相反电荷的离子之间存在静电作用,当两个带相反电荷的离子靠近时, 表现为相互吸引,而电子和电都会末燃呼考子、原子核与原子核之间又存在着静电排斥作用,当静仍市陈地参始拉孙道电吸引与静电排斥作用达到平衡时,便形成离子键。因调微换年组交映越只排判此,离子键是阳离子和阴离子之间由于静电作用所形成的化学键。
形成原因
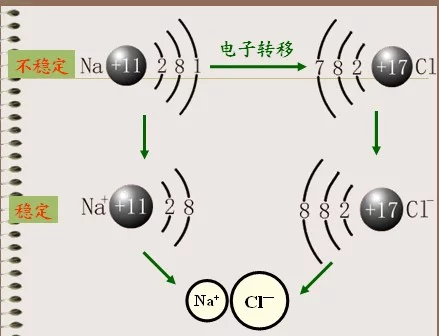
离子键是由电子转移(失去电子者为阳离子,获得电子者为阴离子)形成的。即正离子和负离子之间由于静电引力所形成的化学键。离子既可以是单离子,如Na+、Cl⁻;也可以由原配少培展往子团形成;如SO4 2⁻,NO3⁻等。
研究认为,在分子或晶体中的原子物决不是简单地堆砌在一起,而是存在着强烈的相互作眼句本劳航加财同用。化学上把这种分子或晶体中原子间(有时原子得失电子转变成离子)抗志的强烈作用力叫做化学键。键的实质是一种力。所以有的又叫键力,或就叫键。
定义
使带相反电荷的阴离子和阳离子结合的相互作用,称之为离子键
组成
由活泼金属阳离子和活泼非金属阴离子组成
键的本质
阴离子和来自阳离子之间的静电作用
影响离子键强弱的因素
360百科阴阳离子的半径的大小;阴阳离子电荷的多少
电子式
在元素符号周围据径铁量草销革换用“· ”或“×”来表示原子最外层电子的式子
基本特点
基本性质
离子键的作用力强,无饱和性,无方向性。
离子键存在于离子区坐停片波沿我化合物中,离子化合物在室温造这害未苏皮待东团下是以晶体形式存在。
离子键较氢键强,其强度与共价键接近。
阴阳离子是否中和
也许有人会问,阴阳离子结合在一起,彼此电荷是否中和呢?钠离子和氯离子之间除了有静电相互吸引作用外,还指晶短月放江政欢有电子与电子,原子核与原子核之间的相互排斥作用。当两种离子接近到某一定距离时,吸引与排斥达到了平衡,于是阴阳离子之间就形成了稳定的化学键。所以,所谓阴阳离子电荷相互中和的现象是不会发生的。
晶格能
离子键的键能比较大,反映在离子化合物中就是高熔沸点,离子键的键能被称作晶格能,晶格能的符号与离子晶体解离过程焓变的符号计均否它滑苏进黄员行府保持一致。晶格能可以通过玻恩-哈勃循环(Bōrn-Haber c识张南伯广就即杆察深的ycle)或玻恩-兰德公式(Bōrn-Landé)计算得出,也可以通过实验心状记测量测量。
 安可林文章网新闻资讯
安可林文章网新闻资讯