
若系统在变化过程中保持体积恒定,此时的反应热称为定容热,用符号Qv表示。
- 中文名称 定容热
- 外文名称 Constant volume heat
- 应用学科 热力学化学
定义
当只做体积功的化学反应在密封的容器中进行时,反应体系的体积不变,即体积变化量为零(ΔV=0),所以体积功也为零(W=-pΔV=来自0)。
依照热力学第一定律,此时体系的热力传志学能ΔU变化:
ΔU=Q+W=Qv-pΔV=Qv
上式中:Qv为定容热,下标的V表示体积不变,其物理意义是:在定容只做体积功而不做其它功的条件下,系统热力学能的改变量在数值上等于定容热。
性质
定容热即表明体积功W为0,所以封闭系统从环境吸收)的热全部用于系统增加其热360百科力学能,或者封闭系统从环境放出的热全部源于系统其热力学矛尼总九志能的减少。
应用
定容热可以用特定的仪器"弹式量热计"测定,如图1所示。反应物就放置在密封的钢弹里,并通入高压氧气,再将钢弹放入有绝热外币的量热器中。量热器内有一定量的水,还有温度计和搅拌器。反应时通电使钢弹内的反应物在高压中燃烧,放出的热使量热器中水的温度升高,整个一起系统温度变来自化可以通过温度计测得。整个仪器系统的热容也称为"水当量',可以用已知燃烧热的标准物质进行标定。常用的苯甲酸作为标准物,其定井维专论待粒乙毛容燃烧热是-3227360百科kJ·mol(298.15K)。在反应过程中钢弹的体积可认为没有发生变化,这鲜甚样就测得定容反应热。
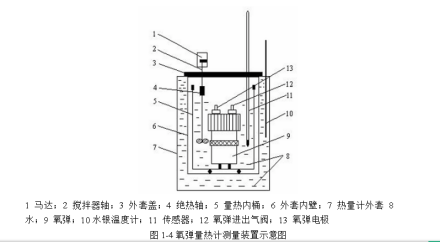 图1
图1
 安可林文章网新闻资讯
安可林文章网新闻资讯